carenza magnesio selenio iodio zinco
MAGNESIO, SELENIO, IODIO E ZINCO
carenza magnesio selenio iodio zinco
carenza magnesio selenio iodio zinco
Le 4 carenze più comuni (e meno riconosciute) nella popolazione sono quelle da magnesio, selenio, iodio e zinco. La quantità necessaria di detti minerali può anche essere molto piccola, tuttavia la sua presenza è di enorme impatto sulla salute. Basti pensare che:
- l’intero sistema nervoso si basa sulla trasmissione di impulsi elettrici;
- tutti i muscoli dipendono dalla presenza di minerali in una certa quantità;
- l’azione svolta dalle molecole di acqua all’interno dell’ organismo è permessa dal fatto che vi sono certi minerali.
I segnali elettrici giocano un ruolo fondamentale:
- nel controllo del battito cardiaco,
- nella regolazione degli ormoni,
- nel trasferimento delle informazioni tra le cellule nervose ed il sistema muscoloscheletrico.
È possibile misurare l’elettricità del corpo attraverso strumenti come l’ECG e l’EEG. La misurazione è possibile in quanto le cellule hanno un loro potenziale di membrana dato dalla differenza tra la carica elettrica interna ed esterna della cellula. Il range varia dai 70 ai 90 millivolt e dà fondamentali indicazioni sulla stessa “vitalità” della cellula.
Magnesio, selenio, iodio e zinco, per un motivo o per un altro, sono carenze molto diffuse nella popolazione, anche perché
- i deficit non vengono, di routine, ricercati (vd analisi del sangue),
- tali sostanze sono meno rappresentati nella nostra alimentazione rispetto al passato, anche a causa di impoverimento delle terre coltivate oppure dell’utilizzo di concimazioni che non ne prevedono la presenza.
1carenza magnesio selenio iodio zinco
1. CARENZA DI MAGNESIO
ll magnesio (Mg) ha una fondamentale importanza: un organismo adulto contiene circa 22-26 g di Mg, di cui il 60% si trova nello scheletro (combinato a calcio e fosforo), mentre ben il 39% si trova dentro le cellule, il 20% nei muscoli striati e l’1% negli spazi extracellulari.
carenza magnesio selenio iodio zinco
Il magnesio è coinvolto:
- nella sintesi e nell’utilizzo dell’ATP (adenosina-tri-fosfato) che è l’energia della cellula (poiché in questi processi la forma attiva dell’ATP è complessata con lo ione magnesio Mg++),
- nel DNA,
- nel’RNA,
- nella sintesi e nella duplicazione degli acidi nucleici.
- nella trasmissione sinaptica cerebrale,
- nell’equilibrio del sistema nervoso,
- nei processi di glicolisi e di gluconeogenesi,
- nella salute dei muscoli,
- nella funzionalità delle adrenali (ghiandole implicate nella reazione agli stress),
- nella produzione di serotonina (il cd “ormone della felicità”).
Circa 325 enzimi richiedono l’intervento degli ioni Mg per svolgere la propria azione.
Secondo alcune indagini, carenze lievi di Mg coinvolgerebbero circa il 70/80% della popolazione occidentale. Quando, viceversa, si riscontrano esami del sangue con carenze di potassio, si può con certezza evincere che il Mg cellulare sia ai minimi inferiori, e si ha già un danno a livello cellulare (tra l’altro, i supplementi di potassio, oltre ad essere pericolosi tante volte, sono inutili senza supplementi di Mg).
carenza magnesio selenio iodio zinco
Sintomi da carenza di Mg:
- ansia, stanchezza, astenia, apatia,
- crampi, convulsioni, tremori,
- vertigini, sindrome di Raynaud,
- nausea, vomito,
- disfunzioni neuromuscolari, fibromialgia,
- calcoli renali,
- dismenorrea, sindrome premestruale, ovaio policistico,
- mal di testa,
- disfunzioni cardiovascolari, aritmia, palpitazioni, etc,
- disfunzioni metaboliche (ipercolesterolemia, ipertensione, etc)
- colon irritabile, ph acido, allergie, depressione, insonnia, osteopenia, tossicità.
L’importanza del Mg per il sistema cardio-circolatorio e metabolico:
I problemi cardiaci risultano spesso correlati ad intossicazioni e carenze di minerali che contribuiscono all’ipertensione e ipercolesterolemia. Il magnesio aiuta la disintossicazione cellulare e l’attività enzimatica. In particolare il Mg contribuisce a regolare l’HMG-CoA reductase esattamente con lo stesso processo sfruttato dai farmaci a base di statine, comportando un abbassamento del colesterolo “cattivo” LDL e trigliceridi ed un innalzamento del colesterolo “buono” HDL. Inoltre, altri enzimi strettamente dipendenti da un appropriato livello di Mg concorrono a convertire gli acidi grassi essenziali omega-3 e 6 in prostaglandine anti-infiammatorie.
Inoltre il Mg, essendo miorilassante/vasodilatante, funziona da anti-ischemico. La carenza di magnesio è molto comune nelle persone con problemi cardiaci, come angina, palpitazioni, aritmie, insufficienza circolatoria. Come ogni altro muscolo, anche il cuore deve poter godere di un giusto apporto di magnesio al suo interno; ed è parimenti importante che sia rispettato il rapporto di almeno 3 a 1 con il calcio (vedi sotto). Contestualmente, migliora la flessibilità dei globuli rossi aiutando la circolazione capillare. Va detto che spesso, nei casi di disturbi cardiaci, si ha anche un quadro di ipertensione, spesso affrontato anche con la prescrizione di diuretici che impoveriscono ulteriormente l’organismo di magnesio e di altri sali minerali.
Il Mg, agendo sulle dislipidemie (metabolismo dei grassi), aiuta anche contro le iperglicemie (metabolismo degli zuccheri), nelle quali si ha un aumento del liquido extracellulare ed una conseguente perdita di sodio. Il Mg favorisce la produzione di insulina e aiuta il riequilibrio elettrolitico sodio-potassio, e quindi attenua i problemi di insulinoresistenza e di picchi glicemici. Si riscontra che il 25% dei diabetici soffra di carenza di Mg in forma grave.
Come fattore indispensabile a circa 325 enzimi, il Mg non deve essere carente in caso di infiammazioni e intossicazioni: va usato dunque come “starter” enzimatico in caso di cd “enzimi bloccati”, o anche in fase di deposito di tossine. Ha una azione blandamente chelante anche nei confronti dei metalli pesanti.
Un ausilio anche per il sistema nervoso e la psiche:
Bassi livelli di Mg (e potassio) sono associati a malattie come l’Alzheimer, la sclerosi multipla ed il Parkinson. Carenze di Mg possono essere alla base di disturbi comportamentali, irritabilità, ansia, nervosismo o ipersensibilità anche ai rumori.
Secondo la Dr.sa Carolyn Dean, il Mg giocherebbe un ruolo importante negli attacchi di panico, che poi “esplodono” quando si ha un abbassamento del glucosio nel sangue. Quando ciò accade, le adrenali rilasciano adrenalina per far sì che i depositi di zucchero del fegato vengano immessi nel torrente sanguigno. L’innalzamento repentino degli zuccheri nel sangue provoca una risposta a livello cerebrale, pressorio e cardiaco. A ciò si aggiunge la possibilità di spasmi dati, appunto, dalla carenza di magnesio, insieme ad anomalie nella trasmissione elettrica del sistema nervoso. Tutto ciò sicuramente predispone alla crisi di attacco di panico.
Anche sui più piccoli è importante monitorare i livelli di magnesio: spesso il cosiddetto disturbo da deficit di attenzione viene attenuato implementando l’apporto di questo importante minerale spesso carente. Alcuni studi dimostrano alcuni effetti benefici nei bimbi autistici anche facendo fare loro dei bagni caldi con sali di magnesio ed una dieta che presta attenzione a zuccheri, latticini e glutine.
L’importanza del rapporto calcio-magnesio:
Una giusta presenza di Mg contribuisce a mantenere corretti anche i livelli di calcio (iper- e ipo-calcemia). Supplementi di calcio per osteopenie/osteoporosi o per ridurre l’acidità devono prevedere la concomitante assunzione nell’arco della giornata (in momenti diversi per favorire l’assorbimento di entrambi) di supplementi di Mg. Ricordiamo che il calcio determina contrazione, mentre il magnesio determina rilascio. Il rapporto Mg-Ca dovrebbe essere di almeno 3 a 1 (se non addirittura di 7 a 1), e non viceversa come oggi accade, rischiando:
- calcificazione dei mitocondri deputati alla respirazione cellulare ed alla produzione di ATP.
- problemi di calcoli renali di calcio, calcificazione prostatica,
- contrazioni muscolari,
- problemi cardiocircolatori e ipertensivi.
Come scoprire la carenza di Mg:
I livelli sierici di Mg nel plasma sono in genere di 0,7-1,0 mmol / litro (1,8-2,4 mEq / litro) e rimangono in omeostasi anche quando la frazione intracellulare risulta carente, questo fa sì che si possa avere una carenza importante a livello biologico senza tuttavia che questo emerga da esami del sangue!
carenza magnesio selenio iodio zinco
Quindi, la misurazione della quantità di Mg nel plasma sanguigno non è affatto indicativa, in quanto solo l’1% del magnesio si trova in esso, mentre la maggior parte si trova a svolgere fondamentali funzioni a livello cellulare. La carenza di Mg cellulare può essere testata con la Biorisonanza (Test completi con la biorisonza)
carenza magnesio selenio iodio zinco
Il problema dell’assorbimento di magnesio:
Solo una frazione minoritaria (10-50%) del magnesio assunto (alimenti e integratori) viene assorbita:
- prima il Mg dev’essere “scorporato” dalle sostanze a cui è legato a livello gastrico grazie all’acido cloridrico; per questo i pazienti che assumono antiacidi inibitori della pompa protonica sono esposti ad un maggior rischio di ipomagnesemia. Una insufficienza di acido cloridrico nello stomaco può compromettere l’assorbimento del magnesio.
- successivamente il Mg deve essere effettivamente assorbito dall’intestino tenue (e in misura molto minore dall’intestino colon)
carenza magnesio selenio iodio zinco

Fattori che inibiscono l’assorbimento di Mg:
- FARMACI antiacidi, CERTI antibiotici (tetracicline, gentamicina), diuretici antipertensivi (furosemide, tiazidici), terapie ormonali (anticoncezionale o sostitutiva), neurolettici, salazopirina, chemioterapici (cisplatino), abuso di lassativi;
- ALIMENTAZIONE con eccesso di fitati (troppi cereali integrali e bucce dei legumi senza un preventivo lungo ammollo), ossalati (troppi spinaci assunti con la “loro acqua” e verdure a foglia verde, tè, caffè, cacao), fosfati (formaggi, lieviti, conservanti e stabilizzanti del ph a base di fosfati), grassi nello stesso pasto (per l’azione saponificante sul magnesio), alcool e zuccheri;
- PATOLOGIE come disbiosi croniche, malattie croniche intestinali, coliti, sindrome della permeabilità intestinale, sindrome da malassorbimento;
- altri fattori: dal momento che le ossa contengono più della metà del magnesio corporeo, in caso di necessità, è possibile attingere anche a tale “riserva” favorendo la mobilitazione rispetto alla deposizione. Perciò il metabolismo del Mg è significativamente influenzato anche dal paratormone e dal contenuto plasmatico di vitamina D.
Una volta che il minerale è stato assorbito a livello intestinale, il compito di regolare le riserve corporee di Mg è affidato principalmente al rene, che agisce sulla quantità del minerale escreta con le urine, sfruttando meccanismi analoghi a quelli per l’intestino. Soltanto una quota di Mg viene perduta con la sudorazione.
Il fabbisogno giornaliero:
Per l’uomo adulto, il fabbisogno giornaliero ammonta a 300-500 mg, ma aumenta significativamente in condizioni particolari (aumentata escrezione fecale o renale, aumentato spostamento intracellulare, terapie antiacide con inibitori della pompa protonica, compromissioni renali, uso di diuretici antipertensivi, terapie con certi antibiotici, uso di anticoncezionali ormonali o di terapie sostitutive ormonali, abuso di caffè, di alcool, di zuccheri, dieta iperproteica, etc).
Alimenti ricchi di Mg:
Sono ricchi di Mg i semi amidacei e oleosi – come legumi (azuki, lenticchie, ceci, fave, piselli, ecc.) – la frutta secca (noci, mandorle, semi di zucca, ecc.) e cereali integrali (riso, frumenti antichi, miglio, quinoa, segale ecc) se non si eccede in fitati. Il magnesio abbonda anche in alcune spezie, nei frutti dolci e negli ortaggi, soprattutto a foglia verde, poiché trattasi di un costituente fondamentale della clorofilla.
Purtroppo, nei prodotti comunemente in vendita nei supermercati, però, le quantità di magnesio hanno un 40-60% in meno di magnesio rispetto a venti anni fa a causa del fatto che i concimi industriali sono più improntati su altri minerali e non sul magnesio (vd “Nitroposka”)
carenza magnesio selenio iodio zinco
Infine esistono acque minerali ricche in sali di magnesio (acque magnesiache).
Integratori di magnesio:
In generale, gli integratori contenenti sali organici (come il magnesio lattato, il magnesio citrato, il magnesio succinato, il magnesio aspartato, il magnesio glicinato, il magnesio taurinato, il magnesio diglicinato, il magnesio fumarato, il magnesio ascorbato ecc.) sono assorbiti in percentuali superiori rispetto agli integratori a base di sali inorganici di magnesio contenuti negli integratori (come il cloruro di magnesio, il carbonato di magnesio, magnesio ossido, magnesio solfato ecc.); tra questi ultimi, il Mg cloruro ha dimostrato una biodisponibilità un poco maggiore grazie alla sua notevole solubilità in acqua (infatti, a livello generale, si è visto che all’aumentare della solubilità in acqua di un sale di Mg aumenta anche la sua biodisponibilità). Purtroppo, in letteratura esistono dati piuttosto contrastanti riguardo alle percentuali esatte di assorbimento dei vari sali di Mg, anche a causa delle variabili di assorbimento viste sopra. Secondo alcuni studi, solo il 4% del magnesio assunto sotto forma di Mg ossido verrebbe effettivamente assorbito, mentre per i sali organici (vd diglicinato) le percentuali assorbite sarebbero 2-3 volte maggiori, nell’ordine dell’8-12%.
L’integrazione di Mg va fatta separatamente rispetto a quella di eventuali altri minerali, in particolare il calcio: l’eccesso di uno o più minerali cationici (come calcio, manganese, potassio, ferro, zinco, fosforo e rame) nello stesso pasto, può ridurre l’assorbimento del Mg formando degli aggregati insolubili. Per il rapporto calcio-Mg (almeno 1 a 3), si veda sopra.
Una dieta o terapia integrante il Mg deve essere protratta anche molto a lungo (diversi mesi) affinché i livelli di magnesio cellulare siano nuovamente adeguati.
Si noti che l’aumento eccessivo del magnesio plasmatico o ipermagnesemia è praticamente impossibile da raggiungere con la sola dieta in condizioni di perfetta salute renale.
carenza magnesio selenio iodio zinco
2. CARENZA DI SELENIO
Il selenio (Se) è un non metallo che, seppure in tracce quantificabili come poche decine di microgrammi (μg), è necessario al funzionamento cellulare:
> Ha una funzione ANTIOSSIDANTE, essendo indispensabile alla formazione degli enzimi antiossidanti glutatione perossidasi (GSH-Px) e tioredossina disolfuro reduttasi protettivi delle membrane plasmatiche dai danni da radicali liberi.
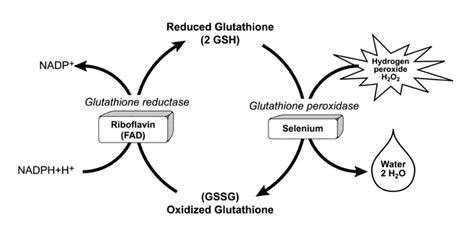
> E’ ANTAGONISTA DEI METALLI PESANTI come il cadmio ed il mercurio: i meccanismi molecolari della tossicità del mercurio si basano sull’inibizione irreversibile dei seleno-enzimi che combattono i danni ossidativi al cervello e nei tessuti endocrini (il tonno rosso, pur accumulando mercurio, non sembra soffrire di avvelenamento contenendo nel sangue alte concentrazioni di selenoneina).
> SUPPORTA LA FUNZIONE TIROIDEA permettendo la conversione della tiroxina (T4) in triiodotironina (T3). Spesso si ha carenza di magnesio nelle tiroiditi autoimmuni di Hashimoto, dove una assunzione di 200 μg di Se può portare ad una riduzione del 21% degli anticorpi anti-TPO.
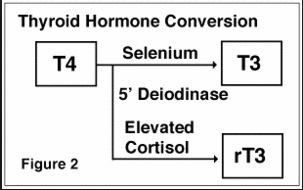
Bassi livelli di Se sono legati a:
- malattie infiammatorie e da danno ossidativo;
- ipotiroidismo;
- disturbi cardiovascolari;
- altre patologie associate al danno da radicali liberi (vd invecchiamento precoce e cataratta);
- secondo alcuni studi epidemiologici si riscontra carenza di Se nel diabete mellito, HIV e tubercolosi;
- maggior rischio di tumore. Studi della Cornell University (USA) proverebbero che con 200 μg di selenio si abbia una diminuzione del 60/70% di diversi tumori;
- l’effetto della carenza cronica di selenio sulla salute umana rimane incerto soprattutto in relazione alla malattia di Kashin-Beck (una malattia del cuore diffusa prevalentemente in alcune aree della Cina i cui terreni sono particolarmente poveri di selenio).
Fabbisogno, alimenti e integrazione:
Per gli adulti, i LARN italiani ele RDA americane consigliano un apporto di selenio pari a 55 μg/die, ma per reintegrare le carenze sintomatiche si usano 100-200 μg/die (la dose tossica è a partire dai 2.000 μg/die) anche perché i seleniti e selenati normalmente contenuti negli integratori alimentari sono meno assorbibili dei selenioamminoacidi solforati (selenio-cisteina e selenio-metionina) dei cibi.
carenza magnesio selenio iodio zinco

Il Se nella dieta è fornito soprattutto dagli alimenti di origine marina e dalle frattaglie. Quindi la carenza è più probabile tra i vegetariani e vegani, oltre che, ovviamente, tra soggetti con funzione intestinale compromessa e malassorbimento. Tra i vegetali che contengono più Se ricordiamo le noci del brasile ed alcuni cereali; anche certi funghi sono ricchi di Se (bisogna però ricordare che il livello di questo minerale nei vegetali e nei funghi è generalmente proporzionale alla sua abbondanza nel terreno). Le famose patate al Se vengono prodotte arricchendo del minerale il suolo durante la concimazione; crescendo in un ambiente ricco di Se, le patate accumulano maggiori quantità del minerale; ciò nonostante, la sua effettiva biodisponibilità ed i relativi – possibili – benefici per la salute sono ancora da chiarire.
carenza magnesio selenio iodio zinco
3. CARENZA DI IODIO
Lo iodio è un micronutriente essenziale della famiglia degli alogeni (si veda meglio la TABELLA-1 più in basso); è presente nell’organismo in piccole quantità, ma è indispensabile non solo per la tiroide (come di solito si sostiene dal momento che gli ormoni T4 e T3 tiroidei sono costituiti per il 65% del loro peso molecolare dallo iodio), ma anche per molti altri tessuti. Infatti solo il 30% dello iodio presente nel corpo umano è riferibile alla tiroide; bel il 70% di esso è invece distribuito in altri tessuti: occhi, ghiandole mammarie, mucosa gastrica, cervice uterina, ghiandole salivari, pareti delle arterie…
carenza magnesio selenio iodio zinco

Calcolare, dunque la dose giornaliera raccomandata solo sul fabbisogno tiroideo, come solitamente si fa, è molto rischioso!
Si stima infatti che a livello globale circa 2 miliardi di persone soffrano di carenze iodiche, di cui circa 1/3 in età scolare (World Health Organization, 2007).
Conseguenze carenza di iodio:
- compromissione della funzionalità tiroidea (ipotiroidismo, disfunzioni metaboliche, deficienza nell’età della crescita, gozzo, etc);
- sintomi connessi all’ipotiroidismo come stanchezza cronica, abulia, sonnolenza, abbassamento del metabolismo basale, dismenorrea, amenorrea, etc.;
- i noduli tiroidei sono favoriti da carenze minerali (iodio, selenio, magnesio);
- possibili connessioni con il cancro alla mammella: la donna iodo-carente può sviluppare un gozzo e iperplasia tiroidea in gravidanza e allattamento, ed è più soggetta a patologia mammaria fibrocistica. Studi scientifici condotti su animali dimostrano che la carenza di iodio, sia connessa alla dieta sia di origine farmacologica, può portare ad atipia mammaria e ad aumento del rischio di cancro mammario. Test di laboratorio hanno dimostrato che l’effetto dello iodio nel tumore al seno è in parte dipendente dalla funzione tiroidea e che lo iodio inibisce l’avanzamento del tumore attraverso la modulazione degli ormoni estrogenici. L’analisi genica di linee cellulari di tumore al seno ormono-sensibile ha mostrato che iodio e composti contenenti iodio alterano l’espressione genica e inibiscono la risposta estrogenica attraverso l’up-regulation di proteine coinvolte nel metabolismo degli estrogeni.
- possibili connessione con il cancro allo stomaco: alcuni ricercatori hanno trovato una correlazione epidemiologica tra carenza di iodio, gozzo e cancro gastrico. Dopo implementazione della iodo-profilassi è stata riportata una riduzione della mortalità per cancro gastrico. Il meccanismo d’azione proposto per questa azione è dato dall’azione antiossidante dello iodio nella mucosa gastrica, che può detossificare composti tossici come i ROS e il perossido di idrogeno.
Attività antiossidante, antibiotica e protettiva dalla radioattività:
Secondo le ultime ricerche lo iodio avrebbe anche una importantissima attività antiossidante, ma sono necessari ulteriori studi per comprendere esattamente il suo meccanismo d’azione. Secondo queste recenti acquisizioni lo iodio sarebbe in grado di proteggere l’organismo dai danni dell’ipercolesterolemia e da molte malattie cardiovascolari (aterosclerosi ed ipertensione).
Ben conosciuta, invece, è l’ATTIVITA’ ANTIBIOTICA/ANTIVIRALE/ANTIMICOTICA che comunque livelli più elevati di iodio svolgono all’interno dell’organismo. Anche nella conoscenza popolare, si sa che la tintura di iodio o il famoso “Betadine” sono potenti barriere verso gli stati infettivi.
Lo iodio uccide il 90% di batteri, virus, protozoo e muffe in circa soli 90 secondi.
Inoltre purtroppo stenta ad affermarsi nel nostro paese la consapevolezza che maggiori livelli di iodio nell’alimentazione o grazie all’integrazione, svolgono una importante attività di PROTEZIONE DA DANNI DA RADIOATTIVITA’ che colpiscono la tiroide stessa, in particolare nei confronti dello iodio radioattivo. Maggiori quantità di iodio diminuiscono fortemente la possibilità che lo iodio radioattivo si leghi alla tiroide ed alle altre ghiandole al posto dello iodio non radioattivo. Non è un caso che in Giappone la dose giornaliera raccomandata di iodio sia quasi cento volte maggiore di quella raccomandata in Italia: ben 12,5 mg (milligrammi e non microgrammi)
La dose raccomandata di iodio:
In Italia le RDA – soltanto ai fini della funzionalità tiroidea – consigliano un apporto giornaliero (nell’adulto) di almeno 150 µg (microgrammi) (molti studi in realtà parlano di ALMENO 200 µg die); per assicurare un normale sviluppo del bambino, per le donne in gravidanza e durante l’allattamento, le RDA consigliano di assumerne rispettivamente almeno 220 µg/die e 300 µg/die. Tuttavia, come sopra accennato, queste RDA fanno riferimento ad un apporto di iodio sufficiente per la sola funzione tiroidea e non anche per gli altri tessuti del corpo, ove lo iodio, ricordiamo, è rappresentato al 70% del totale nell’organismo. Questo fa sì che, ad una tendenziale carenza generalizzata nella popolazione dovuta alla sempre maggiore scarsità dell’oligoelemento nel cibo, si aggiunge l’ignoranza di non considerare integrazioni più importanti che supportino l’organismo anche nelle altre funzioni cui lo iodio presiede: formazione e mantenimento del sistema cognitivo, equilibrio ormonale, funzione antimicrobica, protezione cardiovascolare, protezione verso alcuni tumori e protezione verso la radioattività.
Per quanto riguarda i livelli tossici di iodio, ad oggi non ci sono indicazioni precise. Sappiamo che un eccesso di iodio disturba la tiroide e può provocare alcune forme di ipertiroidismo; il rischio, in tal senso, risulta tanto maggiore quanto minore è il livello di assunzione basale e quanto più l’aumento dell’apporto dietetico avviene rapidamente. Per questo motivo, la pericolosità di un eccesso iodico dipende anche dalla popolazione considerata; in genere il limite superiore di tollerabilità è fissato in 500-600 µg/die (ma forse la stima è troppo prudenziale visto le RDA giapponesi).

Le fonti naturali di iodio:
Le fonti più ricche di iodio sono i pesci di mare ed i crostacei; anche le uova, il latte e la carne ne contengono quantità importanti. La fonte vegetale più abbondante di iodio è rappresentata senza dubbio dalle alghe, come il fucus o la laminaria o wakame, che ne contengono quantità fino a 100-1000 volte superiori rispetto al pesce di mare; inoltre nelle alghe spesso è presente anche il selenio, un componente essenziale del sistema enzimatico che trasforma la tiroxina (T4) in triiodotironina (T3). Gli ortaggi possono contenere un discreto quantitativo di iodio soltanto se sono stati coltivati in terreni ricchi di questo minerale (e magari se non si sono bolliti…); purtroppo però pare che negli ultimi trenta anni, la quantità di iodio sia calata dell’83%.
Una politica che è stata adottata per cercare di aumentare la quantità di iodio nell’alimentazione è quella del sale sale arricchito di iodio. Tuttavia, i dati relativi all’efficacia della “iodoprofilassi” sul territorio italiano non sono stati entusiasmanti, anche a causa del contestuale aumento di bromo nell’alimentazione che, essendo “simile” allo iodio, tende a “prenderne il posto” e quindi a diminuirne l’assimilazione ed a creare danni ossidativi (vedi TABELLA-1 sotto). Comunque, per evitare quanto più possibile perdite di iodio, è consigliabile consumarlo crudo (salare gli alimenti dopo la cottura) e conservarlo in luogo fresco al riparo dalla luce e dall’umidità. La cottura che riduce maggiormente il contenuto in iodio degli alimenti è la bollitura (perdita del 60%) e sarebbe quindi da evitare.
L’eccesso di fibra ed alcuni alimenti o farmaci possono comprometterne l’adeguato assorbimento. Ne sono esempi gli antiacidi che contengono alluminio o magnesio, alcuni farmaci antiulcera (come il sucralfato), integratori di fibra, farina di soia, noci ed i supplementi di ferro o calcio.
Va infine notato che l’abuso di fluoro – che è un alogeno, un rifiuto dell’industria nucleare e che si comporta come una neuro tossina – aggiunto nelle acque pubbliche, nei prodotti per denti, nei farmaci come il Prozac (fluoxetina), interferisce nella disponibilità del corpo di usare lo iodio in quanto utilizza gli stessi recettori (come il bromo di cui sopra; vedi anche TABELLA-1 seguente).
4. CARENZA DI ZINCO
Lo zinco (Zn) è un oligoelemento essenziale per la vita degli esseri umani: si trova infatti in tutti gli organi e nei tessuti (principalmente intracellulari) oltre che nei fluidi corporei.
E’ talmente importante che una carenza di zinco nell’età della crescita, condizioni pesantemente la stessa crescita corporea.
- Lo Zn è presente nel cervello, nel pancreas e nel fegato, ma anche nel nucleo di tutte le cellule;
- è coinvolto nella sintesi del DNA e nell’espressione dei geni;
- è un componente di centinaia di complessi enzimatici coinvolti nel metabolismo di proteine, lipidi, carboidrati e acidi nucleici;
- oltre 60 enzimi richiedono la presenza di tale minerale per essere attivati;
- interviene nella catena beta dell’emoglobina;
- è necessario per il funzionamento di diversi ormoni, inclusa l’insulina che regola gli zuccheri nel sangue, gli ormoni tiroidei e quelli sessuali; serve allo sviluppo delle gonadi (ovaie e testicoli);
- è fondamentale nella riparazione dei tessuti e nella guarigione delle ferite;
- sostiene la risposta immunitaria;
- è importantissimo nelle funzioni nervose e della memoria, ed il suo metabolismo è alterato in condizioni di stress fisico o psichico;
- è un antiossidante indiretto di pelle, cartilagini e muscoli.
Pare abbia funzione immunomodulatrice e antivirale:
> La carenza di Zn pare associata a maggiori stati infiammatori in quanto si è visto che lo Zn abbassa i livelli della proteina NF-κB, fattore centrale della risposta immunitaria (vd Studi dell’Università dell’Ohio).
> Il gluconato di Zn è un rimedio contro il raffreddore o anche contro l’influenza in quanto ha un meccanismo di soppressione dell’infiammazione nasale, di inibizione diretta del legame del recettore del rhinovirus e della replicazione rinovirale nella mucosa nasale.
> Inoltre, per le sue proprietà antibatteriche e antivirali, può essere di aiuto nei casi di diarrea e riduce i sintomi della gastroenterite infettiva.
Per esempio, la somministrazione di Zn è una soluzione semplice, economica ed efficacie per il trattamento degli episodi di diarrea nei bambini dei paesi in via di sviluppo. In passato si riteneva necessario aumentare l’apporto di Zn, a causa della diarrea, solo per compensare le perdite fecali. D’altro canto, recenti studi evidenziano che l’integrazione con zinco – ciclo di trattamento da 10 a 14 giorni – possa ridurre la durata e la gravità degli episodi, contribuendo anche a prevenirli fino a tre mesi grazie all’azione antimicrobica diretta esercitata dagli ioni zinco nel tratto gastrointestinale, o dal rilascio di zinco (post-assorbimento) da parte delle cellule immunitarie – tutti i granulociti secernono lo zinco – o da entrambi.
> Lo Zn è inoltre implicato nel funzionamento dell’olfatto e della vista. E’ considerato preventivo contro la degenerazione maculare senile.
> Nei maschi, lo Zn è un elemento importante per la produzione di sperma.
Fabbisogno, alimenti, integrazione e assimilazione di Zn:
Il fabbisogno giornaliero di Zi varia a seconda del sesso e dell’età. Gli uomini hanno bisogno di circa 15 mg di Zn al giorno, mentre le donne circa 10 mg, come i bambini.
Il contenuto di Zn degli alimenti varia notevolmente. Molte fonti di zinco sono rappresentate da carni rosse (specialmente carni d’organo), da frutti di mare (soprattutto ostriche e molluschi), frutta secca e semi, come semi di zucca, semi di girasole, noci, cacao e nel tuorlo d’uovo. I grani interi e le verdure (foglie e radici) rappresentano buone fonti vegetali di zinco, però contengono fitati e fibra che ne riducono l’assorbimento.

Solo il 10%-30% circa dello Zn presente negli alimenti viene assorbito dall’organismo. Inoltre il trattamento termico delle cotture può indurre la formazione di complessi di Znco non assimilabili: ad esempio nella reazione di Maillard (ossia l’interazione di zuccheri e proteine durante la cottura) si formano complessi che inibiscono la bio-disponibilità di assorbimento dello zinco. Tuttavia, esistono delle sostanze endogene che possono promuovere l’assorbimento dello Zn (acido citrico, acido picolinico e prostaglandine, l’istidina, la cisteina, la lisina e la glicina ed anche il glutatione).
Lo Zn inteso come integratiore viene utilizzato principalmente in forma ossidata: ossido di Zn. Probabilmente meno efficacie, ma comunque presente in varie formule, è lo Zi solfato. Sono molto diffuse anche forme di Zn acetato e zinco gluconato. Negli ultimi anni, il progresso tecnologico ha anche permesso di sviluppare un’ulteriore tipologia farmaceutica ridotta a nano particelle (o Zn picolinato), estremamente efficaci. Ha le stesse applicazioni di quello tradizionale ma gode di maggior efficacia. Infatti, le nanoparticelle di ossido di Zn, che hanno una dimensione media tra 20 nm e 45 nm, possono migliorare l’attività antibatterica.
Gli integratori di zinco dovrebbero essere consumati lontano dai pasti, senza contemporaneamente ingerire altri integratori minerali.
Laura Mancini Tamburini – Vietata la riproduzione
Bibliografia
Magnesium by Dr. Carolyn Dean, md. – Francesco Borgese, Gli elementi della tavola periodica. Rinvenimento, proprietà, usi. Prontuario chimico, fisico, geologico, Roma, CISU, 1993, ISBN 88-7975-077-1. – R. Barbucci, A. Sabatini, P. Dapporto, Tavola periodica e proprietà degli elementi, Firenze, Edizioni V. Morelli, 1998 (archiviato dall’url originale il 22 ottobre 2010). – “Magnesium”, pp.190-249 in “Dietary Reference Intakes for Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride”. National Academy Press. 1997. – Romani, Andrea, M.P. (2013). “Chapter 3. Magnesium in Health and Disease”. In Astrid Sigel; Helmut Sigel; Roland K. O. Sigel. Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. 13. Springer. pp. 49–79. – Ismail Y. The underestimated problem of using serum magnesium measurements to exclude magnesium deficiency in adults; a health warning is needed for “normal” results. Clinical Chemistry and Laboratory Medicine. 48(3):323-237. 2010. – Franz KB (2004). “A functional biological marker is needed for diagnosing magnesium deficiency”. J Am Coll Nutr. 23 (6): 738S–41S. – Ayuk J.; Gittoes N.J. (Mar 2014). “Contemporary view of the clinical relevance of magnesium homeostasis”. Annals of Clinical Biochemistry. 51 (2): 179–88. – Ishimi Y. Nutrition and Bone Health. Magnesium and Bone. Clinical Calcium. 20(5):762-767. 2010. – Eby GA. Magnesium for treatment-resistant depression: a review and hypothesis. Medicine Hypothesis. 74(4):649-660. 2010. – Jacka FN. Association between magnesium intake and depression and anxiety in community-dwelling adults: the Hordaland Health Study. Australian-New Zealand Journal of Psychiatry. 43(1):45-52. 2009. – Mathers TW. Oral magnesium supplementation in adults with coronary heart disease or coronary heart disease risk. Journal of the American Academy of Nurse Practitioners. 21(12):651-657. 2009. – Guerrero-Romero F. The effect of lowering blood pressure by magnesium supplementation in diabetic hypertensive adults with low serum magnesium levels: a randomized, double-blind, placebo-controlled clinical trial. Journal of Human Hypertension. 23(4):245-251. 2009. – The use of magnesium in bronchial asthma: a new approach to an old problem. Archivum immunologiae et therapiae experimentalis. 55(1):35-39. 2007. – Sontia B. Role of magnesium in hypertension. Archives of Biochemistry & Biophysiology. 458(1):33-39. 2007. – Evangelopoulos AA. An inverse relationship between cumulating components of the metabolic syndrome and serum magnesium levels. Nutrition Research. 28(10): 659663. 2008. – Rumawas ME. Magnesium intake is related to improved insulin homeostasis in the Framingham offspring cohort. Journal of the American College of Nutrition. 25(6):486492. 2006. Larsson SC. Magnesium intake and risk of type 2 diabetes: a meta-analysis. Journal of Internal Medicine. 262(2):208-214. 2007. – “Magnesium in diet”. MedlinePlus, U.S. National Library of Medicine, National Institutes of Health. 2 February 2016. Retrieved 13 October 2016. – Vitamins and minerals – Others – NHS Choices”. Nhs.uk. 26 November 2012. Retrieved 19 September 2013. – Rayman, Margaret P. (2000). “The importance of selenium to human health“. The Lancet. 356 (9225): 233–41. – Mazokopakis, E. E.; Papadakis, J. A.; Papadomanolaki, M. G.; et al. (2007). “Effects of 12 months treatment with L-selenomethionine on serum anti-TPO Levels in Patients with Hashimoto’s thyroiditis“. Thyroid. 17 (7): 609–612. – Neurotoxicology. 29 (5): 802–811. -Free Radical Biology and Medicine. 75: 95–104. – Post-transcriptional defects of antioxidant selenoenzymes cause oxidative stress under methylmercury exposure. The Journal of Biological Chemistry. 286 (8): 6641–6649. – Protective effect of selenite against methylmercury toxicity: observations concerning time, dose and route factors in the development of selenium attenuation. Industrial Health. 13 (3): 93–99. – Toxicology. 278(1): 112–123. – Journal of Biological Chemistry. 283 (18): 11913–11923. – Retrieved 2009-01-05. – Institute of Medicine. pp. 314–315. – Wilber, C. G. (1980). “Toxicology of selenium“. Clinical Toxicology. 17 (2): 171–230. – Mann, Jim; Truswell, A. Stewart (2002). Essentials of Human Nutrition (2nd ed.). Oxford University Press. – American Journal of Clinical Nutrition. 78 (1): 137–144. – Cancer Epidemiology Biomarkers & Prevention. 19 (9): 2407–2415. R. Barbucci, A. Sabatini e P. Dapporto, Tavola periodica e proprietà degli elementi, Firenze, Edizioni V. Morelli, 1998 (archiviato dall’url originale il 22 ottobre 2010). Francesco Borgese, Gli elementi della tavola periodica. Rinvenimento, proprietà, usi. Prontuario chimico, fisico, geologico, Roma, CISU, 1993, ISBN 88-7975-077-1. – Ahn Byeong-Cheol, Physiologic and False Positive PathologicUptakes on Radioiodine Whole Body Scan (PDF), 2011. – Farmaci in gravidanza – Emilio Arisi – pag 183-184. – Livelli di Assunzione Raccomandati di Nutrienti per la popolazione italaiana (LARN) – Socità Italiana di Nutrizione Umana (S.I.N.U.) – pag 175:179. – Rošin-Grget, K.; Peroš, K; Sutej, I; Bašić, K (Nov 2013). “The cariostatic mechanisms of fluoride”. Acta medica academica. 42 (2): 179–88. – (EN) Zinc Is an Immunomodulator of the NF-κB Pathway in Human Lung Epithelia, Ohio State University Davis Hearth and Lung Research Institute e Ohio State University College of Pharmacy. – Modulation of telomerase activity by zinc in human prostatic and renal cancer cells, Biochem Pharmacol. 2000 Feb 15;59(4):401-5. – Leitzmann MF, et al. Zinc supplement use and risk of prostate cancer, J Nat Cancer Instit 2003;95:1004-07, su dati di una ricerca dello Health Professionals Follow-up Study. – Gli elementi della tavola periodica. Rinvenimento, proprietà, usi. Prontuario chimico, fisico, geologico, Roma, CISU, 1993, ISBN 88-7975-077-1. – R. Barbucci, A. Sabatini e P. Dapporto, Tavola periodica e proprietà degli elementi, Firenze, Edizioni V. Morelli, 1998 (archiviato dall’url originale il 22 ottobre 2010). – Ferracane, Jack L. (2001). Materials in Dentistry: Principles and Applications. Lippincott Williams & Wilkins. pp. 70, 143. – Padmavathy, Nagarajan; Vijayaraghavan, Rajagopalan (2008). “Enhanced bioactivity of ZnO nanoparticles—an antimicrobial study”. Science and Technology of Advanced Materials. 9 (3): 035004. – Bouchez, Colette. “The Lowdown on Mineral Makeup”.
LINK CORRELATI:
- Test completi con la biorisonanza
- Naturopatia & Frequenze
- Alimentazione curativa
- Stress: stanchezza surrenali?
vd a PAG 2 la TABELLA 1: GLI ALOGENI ed il problema della reattività


